Invega Trinza 200mg/mL, caixa com seringa preenchida com 2,625mL de suspensão injetável de liberação prolongada + 2 agulhas
Janssen-Cilag

Invega Trinza 200mg/mL, caixa com seringa preenchida com 2,625mL de suspensão injetável de liberação prolongada + 2 agulhas
Janssen-CilagDose
Quantidade na embalagem
C1 Branca 2 vias (Venda Sob Prescrição Médica - Este medicamento pode causar Dependência Física ou Psíquica)
Não pode ser partido
Temperatura ambiente
Bula do Invega Trinza
Invega Trinza® pertence à classe de medicamentos antipsicóticos e é utilizado para tratar a esquizofrenia em adultos (de 18 anos ou mais). Invega Trinza® é utilizado após você ter sido tratado com a injeção mensal de palmitato de paliperidona por pelo menos 4 meses. Após os seus sintomas terem sido aliviados com o tratamento de injeção mensal, Invega Trinza® é utilizado para manter o transtorno sob controle, isto é, para evitar recaídas. As injeções de Invega Trinza® são administradas uma vez a cada 3 meses. O Invega Trinza® não deve ser usado para tratar pessoas com esquizofrenia com menos de 18 anos de idade.
A esquizofrenia é um transtorno com sintomas que incluem ouvir coisas, ver ou sentir coisas que não existem, crenças errôneas, suspeitas incomuns, tornar-se retraído, discurso incoerente e respostas emocionais/comportamentais reduzidas. As pessoas com este transtorno podem também sentir-se deprimidas, ansiosas, culpadas ou tensas.
O palmitato de paliperidona é hidrolisado à paliperidona. A paliperidona é um antagonista dopaminérgico D2 de ação central com atividade antagonista 5-HT2A serotoninérgica predominante. A paliperidona também é ativa como antagonista nos receptores alfa-1 e alfa-2-adrenérgicos e nos receptores histaminérgicos H1. A paliperidona não apresenta afinidade pelos receptores colinérgicos muscarínicos ou beta-1 e beta2-adrenérgicos. A atividade farmacológica dos enantiômeros (+)- e (-)- da paliperidona é quali e quantitativamente semelhante.
O mecanismo de ação da paliperidona, como ocorre com outros medicamentos eficazes contra a esquizofrenia, é desconhecido. Entretanto, foi proposto que a atividade terapêutica do medicamento em esquizofrenia é mediada por uma combinação de antagonismo de receptor dopaminérgico do tipo 2 (D2) e serotoninérgico do tipo 2 (5HT2A). O antagonismo em receptores diferentes do D2 e do 5HT2A pode explicar parte dos outros efeitos da paliperidona.
Não utilize Invega Trinza® se você sabe que tem alergia (hipersensibilidade) à paliperidona ou a qualquer outro componente de Invega Trinza®, ou à risperidona, que é outro medicamento antipsicótico semelhante à paliperidona. A hipersensibilidade pode ser reconhecida, por exemplo, através da erupção cutânea, coceira, falta de ar ou inchaço da face. Se alguma destas situações ocorrer, entre em contato com o seu médico imediatamente.
Invega Trinza® não deve ser misturado a nenhum outro produto ou diluente e destina-se à administração intramuscular diretamente da seringa em que está embalado.
O kit contém uma seringa preenchida e 2 agulhas de segurança (uma agulha 22G fina de 1½ polegada e uma agulha 22G fina de 1 polegada).
Invega Trinza® deve ser administrado como uma injeção única por um profissional de saúde. Não divida doses em múltiplas injeções.
Invega Trinza® é destinado apenas para uso intramuscular. Injetar lentamente, profundamente no músculo tendo o cuidado de evitar a injeção em um vaso sanguíneo.
Leia as instruções completas antes de usar.
Selecionar a agulha
- A seleção da agulha é determinada pelo local da injeção e pelo peso do paciente.
- Se a administração for uma injeção deltoide:
- Se a administração for uma injeção deltoide uma injeção glútea:
- Se o paciente pesa:
- Menos do que 90 kg Ponta Pink.
- Independentemente do peso do paciente Ponta Amarela.
- 90 kg ou mais Ponta Amarela.
- Menos do que 90 kg Ponta Pink.
Preparar para a injeção
Agite vigorosamente por pelo menos 15 segundos.
Com a ponta da seringa apontando para cima, agite vigorosamente com o punho solto por pelo menos 15 segundos para assegurar uma suspensão homogênea.
Nota: este medicamento requer mais tempo e uma agitação mais vigorosa do que o medicamento injetável mensal de palmitato de paliperidona.
- Prossiga para o próximo passo imediatamente após a agitação. Se mais do que 5 minutos se passaram antes da injeção, agite vigorosamente novamente, com a ponta da seringa apontando para cima, por pelo menos 15 segundos para voltar a suspender a medicação.
Verificar a suspensão
- Após agitar a seringa por 15 segundos, verifique o líquido na janela de visualização. A suspensão deve aparecer uniforme e de cor branco leitosa. Também é normal observar pequenas bolhas de ar.
Abrir a embalagem da agulha e retirar a tampa
- Primeiro, abra a embalagem da agulha até o meio do caminho para retirar a tampa traseira. Coloque em uma superfície limpa. Então, segurando a seringa na posição vertical, torça e puxe a tampa de borracha para remover.
Segurar a embalagem da agulha
- Dobre para trás a tampa da agulha e o plástico da embalagem. Então, segure firme a agulha na tampa através da embalagem, tal como mostrado.
Conectar a agulha
- Segure a seringa apontando para cima. Prenda a agulha de segurança à seringa usando um movimento de torção suave para evitar rachaduras ou danos ao cubo da agulha. Sempre verifique se há sinais de dano ou vazamento antes da administração.
Retirar a tampa da agulha
- Puxe a tampa da agulha em um movimento em linha reta. Não torça a tampa da agulha, pois isso pode soltar a agulha da seringa.
Remover as bolhas de ar
- Segure a seringa na posição vertical e bata gentilmente para que as bolhas de ar subam para o topo.
- Retire o ar empurrando a haste do êmbolo para cima cuidadosamente até que uma gota de líquido saia da ponta da agulha.
Injetar

Injetar a dose
- Injete lentamente todo o conteúdo da seringa por via intramuscular, em profundidade no músculo deltoide ou no músculo glúteo escolhido. Não administrar por qualquer outra via.
Após a aplicação da injeção

Proteger a agulha
- Após o término da injeção, use o polegar ou uma superfície plana para ativar o sistema de proteção da agulha. A agulha estará protegida quando se ouvir um "clique".
Descartar corretamente
Descarte a seringa e as agulhas não utilizadas em recipientes próprios para o descarte deste tipo de material.
As agulhas de segurança são projetadas especificamente para uso com Invega Trinza®. As agulhas não utilizadas devem ser descartadas e não guardadas para utilização futura.
Posologia Invega Trinza
Invega Trinza® deve ser utilizado apenas após o estabelecimento do tratamento adequado do medicamento injetável de palmitato de paliperidona mensal por pelo menos quatro meses. A fim de estabelecer uma dose de manutenção consistente, é recomendado que as últimas duas doses da injeção mensal tenham a mesma dosagem antes do início de Invega Trinza®.
Iniciar Invega Trinza® no momento em que a próxima dose mensal de palmitato de paliperidona estiver programada, com uma dose de Invega Trinza® baseada na dose da injeção mensal anterior, conforme mostrado na Tabela 1. Invega Trinza® pode ser administrado até 7 dias antes ou depois da data mensal da próxima dose programada de palmitato de paliperidona mensal.
Tabela 1 - Conversão da última dose mensal do medicamento injetável palmitato de paliperidona para o medicamento injetável palmitato de paliperidona trimestral (Invega Trinza®) usando 3,5 como um multiplicador:
| Se a última dose da injeção mensal de palmitato de paliperidona for: | Iniciar Invega Trinza® com a seguinte dose: |
| 50 mg | 175 mg |
| 75 mg | 263 mg |
| 100 mg | 350 mg |
| 150 mg | 525 mg |
A conversão de 25 mg do medicamento injetável mensal de palmitato de paliperidona não foi estudada.
Após a dose inicial de Invega Trinza®, este deve ser administrado a cada 3 meses. Se necessário, o ajuste da dose pode ser realizado a cada 3 meses, em incrementos dentro da faixa de 175 mg a 525 mg, com base na tolerabilidade individual do paciente e/ou na eficácia. Devido à natureza de ação prolongada de Invega Trinza®, a resposta do paciente a uma dose ajustada pode não ser evidente durante vários meses.
Informação de administração
Medicamentos de uso parenteral devem ser inspecionados visualmente antes da administração em relação às partículas estranhas e à alteração da cor. Em até cinco minutos antes da administração de Invega Trinza® no paciente, é importante agitar a seringa vigorosamente durante pelo menos 15 segundos para assegurar a homogeneidade da suspensão.
Invega Trinza® destina-se exclusivamente ao uso intramuscular. Não administrar por via intravenosa ou subcutânea. Evitar a administração inadvertidamente em um vaso sanguíneo. As injeções devem ser administradas apenas por um profissional de saúde. Administrar a dose em uma única injeção. Não administrar a dose em injeções divididas. Injetar lenta e profundamente no músculo deltoide ou glúteo.
Invega Trinza® deve ser administrado utilizando somente as agulhas que são fornecidas na embalagem de Invega Trinza®. As agulhas da embalagem do medicamento injetável mensal de palmitato de paliperidona ou outras agulhas comercialmente disponíveis não devem ser usadas na administração de Invega Trinza®.
O tamanho da agulha recomendado para a administração de Invega Trinza® no músculo deltoide é determinado pelo peso do paciente. Para pacientes ≥ 90 kg de peso corpóreo, recomenda-se a agulha de 1 ½ polegadas, calibre 22. Para pacientes < 90 kg, recomenda-se a agulha de 1 polegada, calibre 22. Administrar no centro do músculo deltoide. As injeções devem ser alternadas entre os dois músculos deltoides.
O tamanho da agulha recomendado para a administração de Invega Trinza® no músculo glúteo, independentemente do peso corpóreo, é a agulha de 1½ polegada, calibre 22. Administrar no quadrante externo superior do músculo glúteo. As injeções devem ser alternadas entre os dois músculos glúteos.
Como a paliperidona é o metabólito ativo da risperidona, deve-se ter cautela quando Invega Trinza® for coadministrado com risperidona ou com paliperidona oral por longos períodos de tempo. Os dados de segurança envolvendo o uso concomitante de Invega Trinza® com outros antipsicóticos são limitados.
Administração incompleta
Para evitar uma administração incompleta de Invega Trinza®, garantir que a seringa preenchida seja agitada vigorosamente por pelo menos 15 segundos nos 5 minutos antes da administração, para assegurar uma homogeneidade da suspensão. No entanto, no caso de uma dose administrada de forma incompleta, não reinjetar a dose remanescente na seringa e não administrar outra dose. Monitorar de perto e tratar o paciente de forma adequada até a próxima injeção trimestral programada de Invega Trinza®.
Populações especiais
Pacientes pediátricos (menores de 18 anos de idade)
A segurança e a eficácia de Invega Trinza® em pacientes menores de 18 anos ainda não foram estudadas.
Pacientes idosos (65 anos ou mais)
Em geral, a dose recomendada de Invega Trinza® para pacientes idosos com função renal normal é a mesma utilizada para os pacientes adultos mais jovens com função renal normal. Como os pacientes idosos podem apresentar função renal reduzida, verificar as recomendações posológicas em pacientes com comprometimento renal.
Pacientes com comprometimento renal
Invega Trinza® não foi sistematicamente estudado em pacientes com comprometimento renal. Para pacientes com comprometimento renal leve (depuração de creatinina ≥ 50 a < 80 mL/min), o ajuste da dose é feito no início do tratamento com o medicamento injetável mensal de palmitato de paliperidona. Não é necessário ajuste da dose de Invega Trinza®. A transição para Invega Trinza® é realizada com uma dose na razão 3,5 para 1 do medicamento injetável mensal previamente estabilizado de palmitato de paliperidona, conforme descrito anteriormente. A dose máxima recomendada de Invega Trinza® em pacientes com comprometimento renal leve é de 350 mg.
Invega Trinza® não é recomendado a pacientes com comprometimento renal moderado ou grave (depuração de creatinina < 50 mL/min).
Pacientes com comprometimento hepático
Invega Trinza® não foi estudado em pacientes com comprometimento hepático. Com base em um estudo com paliperidona oral, nenhum ajuste de dose é necessário em pacientes com comprometimento hepático leve ou moderado. A paliperidona não foi estudada em pacientes com comprometimento hepático grave.
Outras populações
Não é recomendado o ajuste da dose de Invega Trinza® com base no sexo, na raça ou no hábito de fumar.
Troca a partir de outros medicamentos antipsicóticos
Invega Trinza® deve ser utilizado somente após o paciente ter sido tratado de forma adequada com o medicamento injetável mensal de palmitato de paliperidona por pelo menos 4 meses.
Se Invega Trinza® for descontinuado, as suas características de liberação prolongada devem ser consideradas. Conforme recomendado com outros antipsicóticos, a necessidade do uso de medicação para o tratamento de sintomas extrapiramidais (SEP) deve ser periodicamente reavaliada.
Troca de Invega Trinza® para medicamento injetável mensal de palmitato de paliperidona
Para a troca de Invega Trinza® para um medicamento injetável mensal de palmitato de paliperidona, o medicamento injetável mensal de palmitato de paliperidona deve ser administrado no momento em que a próxima dose de Invega Trinza® fosse ser administrada usando o equivalente de 3,5 vezes menor que a dose, como mostrado na Tabela 2. O medicamento injetável mensal de palmitato de paliperidona deve então continuar sendo administrado em intervalos mensais.
Tabela 2 – Conversão do último medicamento injetável trimestral (Invega Trinza®) para o medicamento injetável mensal de palmitato de paliperidona usando como fator de conversão de dose de 3,5 vezes:
| Se a última dose de Invega Trinza® for: | Administrar a seguinte dose mensal de palmitato de paliperidona: |
| 175 mg | 50 mg |
| 263 mg | 75 mg |
| 350 mg | 100 mg |
| 525 mg | 150 mg |
A dose de iniciação, como descrito na bula do medicamento injetável mensal de palmitato de paliperidona, não é necessária.
Troca de Invega Trinza® para comprimidos orais de paliperidona de liberação prolongada
Para trocar de Invega Trinza® para comprimidos orais de paliperidona de liberação prolongada, a dosagem diária dos comprimidos de paliperidona de liberação prolongada deve ser iniciada três meses após a última dose Invega Trinza® e a transição ao longo dos próximos vários meses após a última dose Invega Trinza® conforme descrito na Tabela 4. A Tabela 3 fornece regimes de conversão para permitir que pacientes previamente estabilizados com diferentes doses de Invega Trinza® possam atingir a exposição de paliperidona semelhante aos comprimidos de paliperidona de liberação prolongada uma vez ao dia.
Tabela 3 - Doses de Invega Trinza® e regimes de conversão de dose única diária de paliperidona de liberação prolongada necessários para atingir exposições semelhantes de paliperidona*:
| - | Semanas desde a última dose de Invega Trinza® | |||
| - |
≥ 3 meses até |
> 18 semanas até ≤ 24 semanas |
> 24 semanas | |
| Última dose de Invega Trinza® | Dose diária oral de comprimidos de liberação prolongada de paliperidona | |||
| 175 mg | 3 mg | 3 mg | 3 mg | |
| 263 mg | 3 mg | 3 mg | 6 mg | |
| 350 mg | 3 mg | 6 mg | 9 mg | |
| 525 mg | 6 mg | 9 mg | 12 mg | |
* As doses orais de comprimidos de liberação prolongada de paliperidona devem ser individualizadas, levando-se em consideração a razão da troca, a resposta ao tratamento prévio de paliperidona, a gravidade dos sintomas psicóticos e/ou a tolerabilidade.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
Janela posológica
O esquecimento de doses de Invega Trinza® deve ser evitado. No entanto, em ocasiões excepcionais, você pode receber a injeção até 2 semanas antes ou depois da data trimestral.
Esquecimento de dose há mais de 3 meses e meio até 4 meses
Se mais de 3 meses e meio (até 4 meses) se passaram desde a última injeção de Invega Trinza®, a dose previamente administrada de Invega Trinza® deve ser administrada logo que possível, em seguida, continuar com as injeções trimestrais seguintes a esta dose.
Esquecimento de dose não administrada há mais de 4 meses até 9 meses
Se mais de 4 meses (até 9 meses) se passaram desde a última injeção de Invega Trinza®, NÃO administre a próxima dose de Invega Trinza®.
Em vez disso, utilizar o regime de reiniciação mostrado na Tabela 4.
Tabela 4 – Regime de reiniciação de Invega Trinza® após esquecimento de dose há mais de 4 meses até 9 meses:
| Última dose trimestral do medicamento injetável Invega Trinza® | Administrar o medicamento injetável mensal de palmitato de paliperidona, duas doses no intervalo de uma semana (no músculo deltoide) | Em seguida, administrar uma dose do medicamento injetável Invega Trinza® trimestral (no músculo deltoidea ou glúteo) | |
| - | Dia 1 | Dia 8 | Um mês após o Dia 8 |
| 175 m | 50 mg | 50 mg | 175 mg |
| 263 mg | 75 mg | 75 mg | 263 mg |
| 350 mg | 100 mg | 100 mg | 350 mg |
| 525 mg | 100 mg | 100 mg | 525 mg |
a Vide instruções de uso para seleção da agulha baseada no peso corpóreo para injeção no músculo deltoide.
Esquecimento de dose há mais de 9 meses
Se mais de nove meses se passaram desde a última injeção de Invega Trinza®, reiniciar o tratamento com o medicamento mensal injetável de palmitato de paliperidona, conforme descrito na bula deste produto. Invega Trinza® pode então ser retomado após você ter sido tratado de forma adequada com o medicamento mensal injetável de palmitato de paliperidona durante pelo menos 4 meses.
Em caso de dúvidas, procure orientação do farmacêutico, de seu médico ou do cirurgião-dentista.
Síndrome Neuroléptica Maligna
A Síndrome Neuroléptica Maligna (SNM), caracterizada por hipertermia (temperatura elevada), rigidez muscular, instabilidade autonômica, alteração da consciência e os níveis séricos elevados de creatinofosfoquinase, foi relatada com antipsicóticos, incluindo a paliperidona. Outros sinais clínicos podem incluir mioglobinúria (rabdomiólise - lesão muscular) e insuficiência renal aguda. Se você desenvolver sinais ou sintomas indicativos de SNM, todos os antipsicóticos, inclusive o Invega Trinza®, devem ser descontinuados. Deve-se considerar a natureza da ação prolongada de Invega Trinza®.
Discinesia Tardia/Sintomas extrapiramidais
Os medicamentos com propriedades antagonistas do receptor dopaminérgico são associados à indução de discinesia tardia, caracterizada por movimentos involuntários rítmicos, predominantemente da língua e/ou da face. Se aparecerem sinais e sintomas de discinesia tardia, a descontinuação de todos os medicamentos antipsicóticos, inclusive Invega Trinza®, deve ser considerada. Deve-se considerar a natureza da ação prolongada de Invega Trinza®.
Sintomas extrapiramidais e psicoestimulantes
É necessária precaução em pacientes que receberam concomitantemente psicoestimulantes (por exemplo, metilfenidato) e paliperidona, uma vez que podem surgir sintomas extrapiramidais quando se ajusta um ou ambos os medicamentos. A retirada gradual de um ou ambos dos tratamentos deve ser considerada.
Intervalo QT
Como ocorre com outros antipsicóticos, o médico deve ter cautela ao prescrever Invega Trinza® a pacientes com histórico de arritmias cardíacas, a pacientes com síndrome de QT longo congênita e com o uso concomitante de medicamentos conhecidos por prolongar o intervalo QT.
Reações de hipersensibilidade
As reações anafiláticas em pacientes que previamente tenham tolerado risperidona oral ou paliperidona oral foram muito raramente relatadas durante a experiência pós-comercialização com o medicamento injetável mensal de palmitato de paliperidona.
Caso ocorram reações de hipersensibilidade, o médico deve descontinuar o uso de Invega Trinza®, iniciar medidas gerais de suporte, conforme clinicamente apropriado, e monitorar você até que os sinais e sintomas desapareçam.
Hiperglicemia e diabetes mellitus
Hiperglicemia (açúcar elevado no sangue), diabetes mellitus e exacerbação de diabetes pré-existente foram relatados durante o tratamento com medicamentos antipsicóticos. A avaliação da relação entre o uso de antipsicóticos atípicos e anormalidades da glicose é complicada pela possibilidade de um aumento do risco de diabetes mellitus em pacientes com esquizofrenia e pela crescente incidência de diabetes mellitus na população geral. Por não ser algo claro, não se entende completamente a relação entre o uso de antipsicóticos atípicos e os eventos adversos relacionados à hiperglicemia. Qualquer paciente tratado com antipsicóticos atípicos, incluindo Invega Trinza®, deve ser monitorado quanto a sintomas de hiperglicemia e diabetes mellitus.
Ganho de peso
Foi observado ganho de peso com o uso de antipsicóticos atípicos. Recomenda-se monitoramento clínico do peso.
Hipotensão ortostática
A paliperidona pode induzir à hipotensão ortostática (queda súbita de pressão ao levantar-se) em alguns pacientes devido ao seu efeito bloqueador alfa-adrenérgico. Invega Trinza® deve ser usado com cautela em pacientes com doença cardiovascular conhecida (por exemplo, insuficiência cardíaca, infarto ou isquemia do miocárdio, anormalidades de condução), doença vascular cerebral ou condições que predispõem o paciente à hipotensão (por exemplo, desidratação, hipovolemia e tratamento com medicamentos anti-hipertensivos).
Convulsões
Como ocorre com outros antipsicóticos, Invega Trinza® deve ser usado com cautela se você apresenta histórico de convulsões ou outras condições que potencialmente reduzam o limiar de convulsão.
Pacientes idosos com demência
Invega Trinza® não foi estudado em pacientes idosos com demência. No entanto, os pacientes idosos com demência que são tratados com outros tipos semelhantes de medicamentos podem ter um risco aumentado de acidente vascular cerebral ou de morte.
Leucopenia, neutropenia e agranulocitose
Eventos de leucopenia (redução dos glóbulos brancos no sangue), neutropenia (diminuição do número de neutrófilos no sangue) e agranulocitose (diminuição acentuada na contagem de células brancas do sangue) foram relatados com agentes antipsicóticos, incluindo a paliperidona. Agranulocitose foi relatada muito raramente (< 1/10.000 pacientes) durante a vigilância pós-comercialização.
Pacientes com histórico de baixa contagem de células brancas do sangue (CBS) clinicamente significativa ou leucopenia/neutropenia induzida por medicamento devem ser monitorados durante os primeiros meses de tratamento e deve-se considerar a descontinuação de Invega Trinza® ao primeiro sinal de queda clinicamente significativa nas CBS na ausência de outros fatores causadores.
Pacientes com neutropenia clinicamente significativa devem ser cuidadosamente monitorados para febre ou outros sintomas ou sinais de infecção e tratados imediatamente se tais sintomas ou sinais ocorrerem. Pacientes com neutropenia grave (contagem absoluta de neutrófilos < 1 x 109 /L) devem descontinuar Invega Trinza® e ter suas contagens de células brancas (CBS) acompanhadas até sua recuperação.
Deve-se considerar a natureza da ação prolongada de Invega Trinza®.
Tromboembolismo Venoso
Casos de tromboembolismo venoso (TEV) foram relatados com medicamentos antipsicóticos. Uma vez que os pacientes tratados com antipsicóticos frequentemente apresentam fatores de risco adquiridos para TEV, todos os possíveis fatores de risco para TEV devem ser identificados antes e durante o tratamento com Invega Trinza® e as medidas preventivas devem ser adotadas pelo seu médico.
Doença de Parkinson e Demência com Corpos de Lewy
Os médicos devem avaliar os riscos em relação aos benefícios ao prescrever antipsicóticos, incluindo Invega Trinza®, a pacientes com Doença de Parkinson ou Demência com Corpos de Lewy (DCL), uma vez que ambos os grupos podem correr maior risco de Síndrome Neuroléptica Maligna, bem como ter uma maior sensibilidade aos antipsicóticos. A manifestação desta sensibilidade aumentada pode incluir confusão, embotamento, instabilidade postural com quedas frequentes, além de sintomas extrapiramidais.
Priapismo
Foi relatado que medicamentos com efeitos bloqueadores alfa-adrenérgicos induzem o priapismo (ereção prolongada e/ou dolorosa). Foi relatado priapismo com a paliperidona durante a vigilância pós-comercialização.
Regulação da Temperatura Corpórea
O comprometimento da capacidade de reduzir a temperatura corpórea central foi atribuído a agentes antipsicóticos. Recomenda-se ao médico cuidado adequado ao prescrever Invega Trinza® a pacientes que apresentarem condições que podem contribuir para a elevação da temperatura corpórea central, por exemplo, realização de exercícios extenuantes, exposição ao calor intenso, uso de medicamento concomitante com atividade anticolinérgica ou estar sujeito à desidratação.
Efeito antiemético
Foi observado efeito antiemético nos estudos pré-clínicos com a paliperidona. Esse efeito, se ocorrer em humanos, pode mascarar os sinais e sintomas da superdose com certos medicamentos ou de condições como obstrução intestinal, síndrome de Reye e tumor cerebral.
Administração
O medico deve ter cuidado para evitar a injeção inadvertida de Invega Trinza® em um vaso sanguíneo.
Síndrome de Íris Flácida Intraoperatória
Durante uma operação nos olhos por turvação do cristalino (catarata), a pupila (círculo preto no meio do olho) pode não aumentar de tamanho conforme necessário. Além disso, durante a cirurgia, a íris (parte colorida do olho) pode se tornar flácida, provocando danos nos olhos. Informe seu médico que você está fazendo o uso deste medicamento caso esteja planejando uma operação nos olhos.
Efeitos sobre a capacidade de dirigir veículos e utilizar máquinas
Invega Trinza® pode afetar seu estado de alerta mental e a sua visão. Portanto, você deve ser aconselhado a não dirigir nem operar máquinas até que você conheça a sua sensibilidade ao medicamento.
Durante o tratamento, o paciente não deve dirigir veículos ou operar máquinas, pois sua habilidade e atenção podem estar prejudicadas.
Gravidez e Amamentação
Gravidez
A segurança do palmitato de paliperidona administrado por via intramuscular ou da paliperidona por via oral para uso durante a gravidez humana ainda não foi estabelecida.
Um estudo de coorte observacional retrospectivo baseado em uma base de dados de queixas dos EUA comparou o risco de malformações congênitas em partos de recém-nascidos vivos entre mulheres com e sem uso de antipsicóticos durante o primeiro trimestre de gravidez. A paliperidona, o metabólito ativo da risperidona, não foi avaliada especificamente neste estudo. O risco de malformações congênitas com risperidona, após o ajuste das variáveis de confusão disponíveis no banco de dados, foi elevado em comparação com nenhuma exposição antipsicótica (risco relativo = 1,26, IC 95%: 1,02-1,56). Nenhum mecanismo biológico foi identificado para explicar esses achados e os efeitos teratogênicos não foram observados em estudos não clínicos. Com base nos achados deste estudo observacional único, não foi estabelecida uma relação causal entre a exposição in utero à risperidona e malformações congênitas.
Nenhum efeito teratogênico foi observado nos estudos em animal. Os animais de laboratório tratados com dose elevada de paliperidona oral demonstraram discreto aumento dos óbitos fetais. Os parâmetros da gravidez não foram afetados em ratos que receberam a injeção intramuscular mensal de palmitato de paliperidona. As doses elevadas foram tóxicas às mães. Os filhotes não foram afetados nas exposições orais de 20 a 22 vezes a exposição humana máxima de paliperidona oral ou nas exposições intramusculares 6 vezes a exposição humana máxima do medicamento injetável mensal de palmitato de paliperidona.
Recém-nascidos expostos a medicamentos antipsicóticos (incluindo a paliperidona) durante o terceiro trimestre da gravidez correm o risco de apresentar sintomas extrapiramidais e/ou de retirada, que podem variar em severidade após o parto. Estes sintomas nos recém-nascidos podem incluir agitação, hipertonia, hipotonia, tremor, sonolência, dificuldade respiratória ou transtornos alimentares. Uma vez que a paliperidona foi detectada no plasma até 18 meses após a administração de dose única de Invega Trinza®, deve-se considerar a natureza da ação prolongada de Invega Trinza®, já que recém-nascidos podem estar sob risco com a administração de Invega Trinza® antes da gravidez ou durante o primeiro e segundo trimestres.
Invega Trinza® só deve ser usado durante a gravidez se os benefícios superarem os riscos. O efeito de Invega Trinza® sobre o trabalho de parto e sobre o parto em humanos é desconhecido.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Amamentação
Em estudos em animais com a paliperidona e em estudos em humanos com a risperidona, a paliperidona foi excretada no leite. Portanto, as mulheres que estão recebendo Invega Trinza® não devem amamentar. Uma vez que a paliperidona foi detectada no plasma até 18 meses após a administração de uma dose única de Invega Trinza®, deve-se considerar a natureza da ação prolongada de Invega Trinza® já que os lactentes podem estar sob risco com a administração de Invega Trinza® antes da amamentação.
Assim como todos os medicamentos, Invega Trinza® pode causar reações adversas, embora nem todas as pessoas as apresente.
Dados de Estudos Clínicos
As seguintes reações adversas foram observadas em estudos clínicos de Invega Trinza® para prevenção de recaída em pacientes com esquizofrenia:
- Infecções e Infestações: infecção no trato respiratório superior, infecção de trato urinário.
- Distúrbios de Metabolismo e Nutrição: hiperglicemia (açúcar aumentado no sangue), hiperinsulinemia (aumento de insulina no sangue), aumento de peso.
- Distúrbios Psiquiátricos: ansiedade.
- Distúrbios do Sistema Nervoso: acatisia, discinesia, distonia, cefaleia (dor de cabeça), Parkinsonismo, sonolência.
- Distúrbios Cardíacos: taquicardia (batimentos aumentados do coração).
- Distúrbios Vasculares: hipotensão ortostática (queda de pressão ao levantar-se).
- Distúrbios Gastrintestinais: náusea, vômito.
- Distúrbios no Sistema Reprodutivo e Mamário: galactorreia, amenorreia.
- Distúrbios Gerais e Condições no Local de Administração: reação no local da injeção.
Além dessas reações, as seguintes reações adversas adicionais foram relatadas com a paliperidona e/ou risperidona em estudos clínicos:
- Infecções e infestações: acarodermatite, bronquite, celulite, cistite, infecção de ouvido, infecção do olho, influenza, onicomicose, pneumonia, infecção do trato respiratório, sinusite, abscesso subcutâneo, tonsilite.
- Distúrbios sanguíneos e do sistema linfático: anemia, neutropenia, diminuição de célula branca no sangue.
- Distúrbios do sistema imunológico: hipersensibilidade.
- Distúrbios Endócrinos: glicose presente na urina, hiperprolactinemia.
- Distúrbios do Metabolismo e Nutrição: aumento de colesterol sanguíneo, aumento de triglicérides sanguíneo, diminuição de apetite, aumento de apetite, polidipsia, diminuição de peso.
- Distúrbios Psiquiátricos: agitação, anorgasmia, embotamento afetivo, estado de confusão, depressão, insônia, libido diminuída, nervosismo, pesadelo, transtorno do sono.
- Distúrbios do Sistema Nervoso: isquemia cerebral, perturbação da atenção, tontura, tontura postural, disartria, hipoestesia, parestesia, hiperatividade psicomotora, síncope, discinesia tardia, tremor.
- Distúrbios Oculares: conjuntivite, olho seco, glaucoma, aumento da lacrimação, visão turva.
- Distúrbios do Ouvido e Labirinto: dor de ouvido, zumbido, vertigem.
- Distúrbios Cardíacos: bloqueio atrioventricular, bradicardia, distúrbio de condução, eletrocardiograma anormal, prolongamento QT no eletrocardiograma, palpitações, síndrome de taquicardia postural ortostática.
- Distúrbios Vasculares: hipertensão, hipotensão.
- Distúrbios Respiratórios, Torácicos e Mediastinais: tosse, dispneia, epistaxe, congestão nasal, dor faringolaringeal, congestão do trato respiratório.
- Distúrbios Gastrintestinais: desconforto abdominal, dor abdominal, queilite, constipação, diarreia, boca seca, dispepsia, disfagia, flatulência, gastroenterite, dor de dente.
- Distúrbios Hepatobiliares: aumento de gama-glutamiltransferase, aumento de enzimas hepáticas, aumento de transaminases.
- Distúrbios da Pele e do Tecido Subcutâneo: acne, erupção medicamentosa, pele seca, eczema, eritema, prurido, erupção cutânea, urticária.
- Distúrbios Musculoesquelético e do Tecido Conjuntivo: artralgia, dor nas costas, aumento da creatinofosfoquinase sanguínea, rigidez articular, inchaço das articulações, espasmos musculares, fraqueza muscular, dor musculoesquelética, dor no pescoço.
- Distúrbios Renais e Urinários: disúria, polaciúria, incontinência urinária.
- Distúrbios do Sistema Reprodutivo e Mamário: desconforto mamário, aumento mamário, dor mamária, distúrbios de ejaculação, disfunção erétil, ginecomastia, distúrbios menstruais, disfunção sexual.
- Distúrbios Gerais e Condições no Local de Administração: astenia, aumento da temperatura corporal, desconforto no peito, dor no peito, arrepios, síndrome de abstinência de drogas, edema facial, fadiga, marcha anormal, mal-estar, edema, pirexia.
- Lesões, envenenamento e complicações de intervenções: queda.
As reações adversas adicionais relatadas em outros estudos clínicos de paliperidona e risperidona são mostradas a seguir:
- Distúrbios Sanguíneos e do Sistema Linfático: aumento da contagem de eosinófilos.
- Distúrbios do Sistema Imunológico: reação anafilática.
- Distúrbios do Metabolismo e Nutrição: anorexia.
- Distúrbios do Sistema Nervoso: distúrbio do equilíbrio, convulsão, coordenação anormal, nível de consciência deprimido, coma diabético, cabeça hesitante, perda de consciência, Síndrome Neuroléptica Maligna, irresponsivo aos estímulos.
- Distúrbios Oculares: distúrbio no movimento dos olhos, revirar os olhos, hiperemia ocular, fotofobia.
- Distúrbios Cardíacos: arritmia sinusial.
- Distúrbios Vasculares: rubor, isquemia.
- Distúrbios Respiratórios, Torácicos e Mediastinais: disfonia, hiperventilação, pneumonia aspirativa, congestão pulmonar, estertores, respiração ofegante.
- Distúrbios Gastrintestinais: incontinência fecal, fecaloma, obstrução intestinal, língua inchada.
- Distúrbios da Pele e do Tecido Subcutâneo: caspa, hiperqueratose, dermatite seborreica, descoloração da pele.
- Distúrbios Musculoesquelético e do Tecido Conjuntivo: postura anormal, rabdomiólise.
- Distúrbios do Sistema Reprodutivo e Mamário: ingurgitamento mamário, corrimento vaginal.
- Distúrbios Gerais e Condições no Local de Administração: diminuição da temperatura corporal, endurecimento, sede.
Invega Trinza® pode aumentar os níveis de um hormônio chamado prolactina, observado no exame de sangue (que pode ou não causar sintomas). Quando os sintomas da prolactina alta ocorrerem, eles podem incluir: (em homens) inchaço do peito, dificuldade em obter ou em manter ereções ou outra disfunção sexual; (em mulheres) desconforto no peito, perda de leite dos seios, perda de períodos menstruais ou outros problemas com o seu ciclo.
Dados pós-comercialização
Além das reações adversas relatadas durante os estudos clínicos acima descritos, as seguintes reações adversas foram relatadas durante a experiência pós-comercialização com a paliperidona e/ou risperidona. As reações adversas são apresentadas por categoria de frequência com base em taxas de relatos espontâneos.
Reação rara (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento)
- Distúrbios da Pele e do Tecido Subcutâneo: angioedema.
Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento)
- Distúrbios sanguíneos e do Sistema linfático: agranulocitose, trombocitopenia.
- Distúrbios do Metabolismo e Nutrição: diabetes mellitus, cetoacidose diabética, hipoglicemia.
- Distúrbios Psiquiátricos: catatonia, mania, sonambulismo.
- Distúrbios do Sistema Nervoso: disgeusia.
- Distúrbios Cardíacos: fibrilação atrial.
- Distúrbios Vasculares: trombose venosa, embolia pulmonar.
- Distúrbios Respiratórios, Torácicos e Mediastinais: síndrome da apneia do sono.
- Distúrbios Gastrintestinais: pancreatite, íleo paralítico.
- Distúrbios da Pele e do Tecido Subcutâneo: alopécia.
- Distúrbios Renais e Urinários: retenção urinária. Gravidez, puerpério e condições perinatais: síndrome de abstinência neonatal de drogas.
- Distúrbios do Sistema Reprodutivo e Mamário: priapismo.
- Distúrbios Gerais e Condições no Local de Administração: hipotermia, abscesso no local da injeção, celulite no local da injeção, hematoma no local da injeção.
Reação desconhecida (a frequência não pode ser estimada a partir dos dados disponíveis)
- Distúrbios Endócrinos: secreção inadequada do hormônio antidiurético.
- Distúrbios do Metabolismo e Nutrição: intoxicação por água.
- Distúrbios Psiquiátricos: distúrbio alimentar ao sono.
- Distúrbios Oculares: síndrome de íris flácida (intraoperatório).
- Distúrbios Hepatobiliares: icterícia.
- Distúrbios Gerais e Condições no Local de Administração: cisto no local da injeção, necrose no local da injeção, úlcera no local da injeção.
- Distúrbios da Pele e do Tecido Subcutâneo: Síndrome de Stevens-Johnson ou necrólise epidérmica tóxica (erupção cutânea grave ou que pode levar a risco de morte, com bolhas e descamação da pele, que pode começar na região da boca, nariz, olhos e órgãos genitais e se espalhar para outras áreas do corpo).
Muito raramente, casos de reação anafilática após a administração do medicamento injetável mensal de palmitato de paliperidona foram notificados na pós-comercialização em pacientes que previamente toleravam a risperidona oral ou a paliperidona oral.
Atenção: este produto é um medicamento novo e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, informe seu médico ou cirurgião-dentista.
Suspensão injetável de liberação prolongada de palmitato de paliperidona em seringas preenchidas
Kit com uma seringa preenchida de 175 mg, 263 mg, 350 mg ou 525 mg e dois tipos de agulhas 22G fina de 1½ polegada e 22G fina de 1 polegada.
Uso intramuscular.
Uso adulto acima de 18 anos.
Invega Trinza® contém 175 mg, 263 mg, 350 mg ou 525 mg de paliperidona (presente sob a forma de 273 mg, 410 mg, 546 mg ou 819 mg de palmitato de paliperidona, respectivamente).
Excipientes: ácido cítrico monoidratado, macrogol 4000, polissorbato 20, fosfato de sódio monobásico monoidratado, hidróxido de sódio, água para injetáveis.
Como Invega Trinza® deve ser armazenado e administrado por um profissional de saúde, o potencial para a superdose pelos pacientes é baixo.
Em caso de superdose, um ou mais dos seguintes sinais podem ocorrer:
- Redução da consciência, sonolência, tremores excessivos, rigidez muscular excessiva, batimento acelerado do coração e pressão arterial baixa.
Foram relatados casos de condução elétrica anormal no coração (prolongamento do intervalo QT) e convulsão. A superdose pode acontecer se você estiver utilizando outros medicamentos juntamente com Invega Trinza®. Se você apresentar os sintomas acima, entre em contato com o seu médico para que você possa ser tratado por ter recebido excesso de Invega Trinza®.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001 se você precisar de mais orientações.
O médico deve ter cautela ao prescrever Invega Trinza® junto aos medicamentos conhecidos por prolongar o intervalo QT.
Como o palmitato de paliperidona é hidrolisado à paliperidona, os resultados dos estudos com a paliperidona oral devem ser levados em consideração ao avaliar o potencial de interação medicamentosa.
Potencial de Invega Trinza® afetar outros medicamentos
Não é de se esperar que a paliperidona cause interações farmacocinéticas clinicamente importantes com medicamentos metabolizados pelas isoenzimas do citocromo P450. Os estudos in vitro em microssomos hepáticos humanos demonstraram que a paliperidona não inibe consideravelmente o metabolismo dos medicamentos metabolizados pelas isoenzimas do citocromo P450, incluindo CYP1A2, CYP2A6, CYP2C8/9/10, CYP2D6, CYP2E1, CYP3A4 e CYP3A5. Portanto, não é de se esperar que a paliperidona iniba a depuração de medicamentos metabolizados por essas vias metabólicas de maneira clinicamente relevante. Também não é de se esperar que a paliperidona apresente propriedades indutoras enzimáticas.
A paliperidona é um inibidor fraco da glicoproteína P (P-gp) em concentrações elevadas. Não existem dados “in vivo” disponíveis e a importância clínica é desconhecida.
Devido aos efeitos primários da paliperidona sobre o SNC, Invega Trinza® deve ser usado com cautela em combinação a outros medicamentos de ação central e ao álcool. A paliperidona pode antagonizar o efeito da levodopa e de outros agonistas dopaminérgicos.
Devido ao seu potencial de indução da hipotensão ortostática, pode ser observado efeito aditivo ao administrar Invega Trinza® com outros agentes terapêuticos que apresentam esse potencial.
A administração concomitante de comprimidos de paliperidona oral de liberação prolongada no estado de equilíbrio (12 mg uma vez ao dia) com comprimidos de divalproato de sódio de liberação prolongada (500 mg a 2000 mg uma vez ao dia) não afetou a farmacocinética de valproato no estado de equilíbrio.
A interação farmacocinética entre Invega Trinza® e lítio é improvável.
Potencial de outros medicamentos afetarem Invega Trinza®
A paliperidona não é um substrato da CYP1A2, CYP2A6, CYP2C9, CYP2C19 e CYP3A5. Isto sugere que é improvável ocorrer interação com inibidores ou indutores dessas isoenzimas. Embora os estudos in vitro indiquem que a CYP2D6 e a CYP3A4 possam estar minimamente envolvidas no metabolismo da paliperidona, não houve indicações in vitro ou in vivo de que essas isoenzimas tenham um papel importante no metabolismo da paliperidona. Os estudos in vitro demonstraram que a paliperidona é um substrato da P-gp. A paliperidona é metabolizada pela CYP2D6 em extensão limitada. Em um estudo de interação em indivíduos saudáveis, no qual a paliperidona oral foi administrada concomitantemente à paroxetina, um potente inibidor da CYP2D6, não foram observados efeitos clinicamente relevantes sobre a farmacocinética da paliperidona.
A administração concomitante de paliperidona oral de liberação prolongada uma vez ao dia com carbamazepina 200 mg duas vezes ao dia provocou a redução de aproximadamente 37% na Cmáx e na AUC médias no estado de equilíbrio da paliperidona. Esta redução é causada, em grau considerável, pelo aumento de 35% na depuração renal da paliperidona provavelmente como resultado da indução da P-gp renal pela carbamazepina. Uma redução menor da quantidade de fármaco excretada inalterada na urina sugere que houve pouco efeito sobre o metabolismo da CYP ou sobre a biodisponibilidade da paliperidona durante a administração concomitante da carbamazepina. Com a inclusão da carbamazepina, a dose de Invega Trinza® deve ser reavaliada e aumentada, se necessário. Por outro lado, com a descontinuação da carbamazepina, a dose de Invega Trinza® deve ser reavaliada e diminuída, se necessário. Deve-se considerar a natureza da ação prolongada de Invega Trinza®.
A paliperidona, um cátion em pH fisiológico, é excretada principalmente inalterada pelos rins, aproximadamente metade por filtração e a outra metade por secreção ativa. A administração concomitante da trimetoprima, um fármaco conhecido por inibir o transporte renal ativo de cátions, não influenciou a farmacocinética da paliperidona.
A administração concomitante de 12 mg oral de paliperidona de liberação prolongada em dose única e comprimidos de liberação prolongada de divalproato de sódio (dois comprimidos de 500 mg uma vez ao dia) resultou em um aumento de aproximadamente 50% no Cmáx e na AUC de paliperidona, provavelmente como resultado de uma absorção oral aumentada. Como não foi observado nenhum efeito significativo na depuração sistêmica, não é esperada uma interação clinicamente significativa entre comprimidos de liberação prolongada de divalproato de sódio e injeção intramuscular de Invega Trinza®. Esta interação não foi estudada com Invega Trinza®.
A interação farmacocinética entre Invega Trinza® e lítio é improvável.
Uso concomitante de Invega Trinza® com risperidona ou com paliperidona oral
Como a paliperidona é o metabólito ativo da risperidona, deve-se ter cautela quando Invega Trinza® for coadministrado com risperidona ou com paliperidona oral, por um longo período de tempo. Os dados de segurança envolvendo o uso concomitante de Invega Trinza® com outros antipsicóticos são limitados.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Paliperidona deve ser tomado toda manhã com ou sem café da manhã, porém da mesma maneira todos os dias.
Embora a presença ou ausência de alimentos no tempo de administração de Paliperidona possam aumentar ou diminuir a exposição à paliperidona, estas alterações não foram consideradas clinicamente relevantes. Os estudos clínicos que estabeleceram a eficácia e a segurança de Paliperidona foram realizados sem relação com o tempo das refeições.
Resultados de eficácia
Esquizofrenia Adultos
A eficácia de Paliperidona foi estabelecida em 3 estudos clínicos controlados com placebo e com ativo (olanzapina), duplo-cegos, de 6 semanas de duração em pacientes que preenchiam os critérios estipulados pelo “Manual de Transtornos Mentais publicados pela “American Psychiatric Association (DSM-IV-TR)” para esquizofrenia.
O controle ativo foi incluído para fins de sensibilidade do teste. As doses de Paliperidona, que variaram entre os 3 estudos, foram de 3 a 15 mg uma vez ao dia.
A eficácia foi avaliada usando a Escala de Síndrome Positiva e Negativa (PANSS); o desfecho primário foi a redução nos escores totais da PANSS. Uma análise dos subgrupos populacionais não revelou qualquer evidência de resposta diferenciada em relação à idade, raça ou gênero.
Desfechos secundários também foram avaliados, incluindo a escala de Desempenho Pessoal e Social (Personal and Social Performance PSP) e escala de Impressão Clínica Global Gravidade (Clinical Global Impression – Severity: CGI-S). A escala PSP corresponde a um instrumento de avaliação clínica validado que mede quatro áreas de funcionamento pessoal e social (atividades sociais úteis incluindo trabalho, estudo, relacionamentos pessoais e sociais, cuidados pessoais, comportamento perturbado e agressivo).
A escala CGI-S corresponde a uma avaliação global de impressão clínica do investigador em relação à gravidade da doença. Em uma análise com dados agrupados (“pooled data”) destes três estudos, cada dose de Paliperidona apresentou-se de forma superior, ao ser comparado com o placebo em relação ao PSP e CGI-S. Em adição, o efeito em PSP mostrou-se distinto da melhora nos sintomas medidos como desfecho primário (PANSS total).
Em análise posterior da fase aberta de extensão destes três estudos, foi revelado que a dose flexível de Paliperidona (3 a 15 mg, dose diária), por mais de 52 semanas, estava associada com uma contínua melhora na escala PSP.
Em estudo de longo prazo, delineado para avaliar a manutenção de efeito, Paliperidona apresentou-se de maneira significativamente mais eficaz que o placebo para a manutenção do controle dos sintomas e retardando a recorrência da esquizofrenia.
Neste estudo, adultos que preencheram os critérios estabelecidos pela DSM-IV para esquizofrenia e que permaneceram clinicamente estáveis por meio de doses determinadas de Paliperidona, durante um período de 8 semanas de tratamento aberto (doses entre 3 e 15 mg uma vez ao dia), depois de receberem um tratamento para um episódio agudo para as 06 semanas prévias com Paliperidona (doses entre 3 a15 mg uma vez ao dia), foram então aleatoriamente alocados de forma duplo-cega para continuar com Paliperidona, em dose estável, ou placebo, até que fossem observados sintomas de recorrência da esquizofrenia.
O estudo foi interrompido precocemente por motivos de eficácia, quando se atingiram critérios pré-definidos.
Com base em uma análise interna foi demonstrado um tempo significativamente maior para a recorrência em pacientes tratados com Paliperidona, comparados ao placebo (p=0,0053). Baseado em uma análise final e considerando os pacientes incluídos após o ponto de corte utilizado para análise interina, a taxa de eventos recorrentes foi de 22,1% no grupo de Paliperidona, comparada à taxa de 51,5% apresentada pelo grupo placebo.
Uma significativa melhora nos sintomas foi alcançada ao final da fase aberta em estabilização (decréscimo em valores totais em PANSS de 38 pontos, com desvio padrão de ± 16,03); entretanto, após a alocação aleatória para tratamento duplo-cego, os pacientes recebendo placebo deterioraram significativamente mais que pacientes recebendo Paliperidona (p<0,001). Paliperidona também foi significativamente mais efetivo que o placebo na manutenção de desempenho pessoal e social. Durante a fase duplo-cega deste estudo, de acordo com a medida da escala CGI-S, houve uma piora da gravidade total da psicose no grupo placebo, enquanto pacientes tratados com Paliperidona permaneceram clinicamente estáveis.
A redução do risco absoluto (RRA) e número necessário para tratar (NNT), necessários para promover melhora ≥30% no escore total da escala PANSS em 03 estudos clínicos fase III comparativos com placebo (SCH-303 / SCH-304 / SCH-305) são apresentados na tabela abaixo:
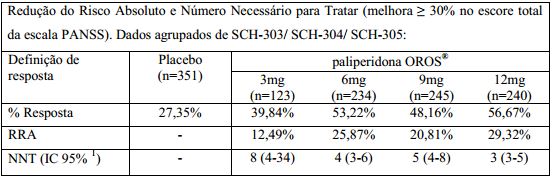 % Resposta: porcentagem de pacientes com melhora de ≥30% no escore total da escala PANSS, da linha de base ao ponto final.
% Resposta: porcentagem de pacientes com melhora de ≥30% no escore total da escala PANSS, da linha de base ao ponto final.
RRA: Redução do Risco Absoluto diferença entre a proporção de pacientes respondendo à paliperidona de liberação prolongada e placebo.
NNT: Número Necessário para Tratar: 1/RRA número de pacientes que necessitariam ser tratados para obter um desfecho positivo adicional que não ocorreria caso o paciente tivesse recebido placebo.
IC: Intervalo de Confiança.
Em resumo, a eficácia e a segurança de Paliperidona foram demonstradas em 03 estudos de fase III, com 06 semanas de duração.
A eficácia de PaliperidonaM na manutenção da estabilidade clínica foi comprovada por um período de até 11 meses. Isto foi demonstrado em um estudo para avaliar a recorrência de sintomas em pacientes com esquizofrenia clinicamente estáveis por um período de 08 semanas.
Esquizofrenia Adolescentes
A eficácia de Paliperidona em pacientes adolescentes com esquizofrenia foi estabelecida em um ensaio clínico randomizado, duplo-cego, em grupos paralelos, controlado por placebo, com duração de 6 semanas e desenho de grupo de tratamento com dose fixa baseado no peso corporal, na faixa de dose de 1,5 a 12 mg/dia.
Os pacientes tinham de 12 a 17 anos de idade e preenchiam os critérios estipulados pelo “Manual de Transtornos Mentais publicados pela “American Psychiatric Association (DSM-IV-TR)” para esquizofrenia, com confirmação do diagnóstico utilizando o questionário “Kiddie Schedule for Affective Disorders and Schizophrenia Present and Lifetime Version (K-SADS-PL)”.
Pacientes elegíveis foram aleatoriamente alocados para 1 dos 4 grupos de tratamento
Um grupo placebo ou grupos de dose baixa, média ou alta de Paliperidona. As doses foram administradas baseando-se no peso corporal para minimizar o risco de exposição de adolescentes com menor peso a doses mais elevadas de Paliperidona.
Pacientes com peso entre 29 kg e 51 kg na linha de base da visita foram aleatoriamente alocados para receber placebo ou 1,5 mg (dose baixa), 3 mg (dose média), ou 6 mg (dose alta) de Paliperidona diariamente, e os pacientes pesando pelo menos 51 kg na linha de base da visita foram aleatoriamente alocados para receber placebo ou 1,5 mg (dose baixa), 6 mg (dose média), ou 12 mg (dose alta) de Paliperidona diariamente.
A dose foi administrada pela manhã, independentemente das refeições.
A eficácia foi avaliada usando PANSS. Este estudo demonstrou a eficácia de Paliperidona em pacientes adolescentes com esquizofrenia, quando administrado em doses diárias de 3, 6 e 12 mg em grupos de tratamento baseados no peso corporal.
A dose mínima efetiva para Paliperidona nesta população foi de 3 mg/dia.
Transtorno esquizoafetivo
A eficácia de Paliperidona (3 mg a 12 mg uma vez ao dia) no tratamento de transtorno esquizoafetivo foi estabelecida em 2 estudos controlados por placebo com duração de 6 semanas em pacientes não-idosos que preencheram os critérios DSM-IV para o transtorno esquizoafetivo, confirmado pela Entrevista Clínica Estruturada paraTranstornos do DSM-IV.
Em um destes estudos, a eficácia foi avaliada em 203 pacientes que foram atribuídos a um dos dois níveis de dose de Paliperidona
6 mg com a opção de reduzir para 3 mg (n = 105) ou 12 mg com a opção de reduzir para 9 mg (n = 98) uma vez ao dia. No outro estudo, a eficácia foi avaliada em 211 pacientes que receberam doses flexíveis de Paliperidona (3 – 12 uma vez ao dia).
Ambos os estudos incluíram pacientes que receberam Paliperidona em monoterapia ou em combinação com antidepressivos e/ou estabilizadores de humor.
A dose foi administrada pela manhã, independentemente das refeições. Os estudos foram realizados nos Estados Unidos, Europa Oriental, Rússia e Ásia.
A eficácia foi avaliada utilizando a Escala da Síndrome Positiva e Negativa (PANSS), um inventário validado de múltiplos itens composto por 5 fatores para avaliar os sintomas positivos, sintomas negativos, pensamentos desorganizados, hostilidade descontrolada / excitação e ansiedade / depressão.
O grupo de doses elevadas de Paliperidona em estudo de 2 níveis de dose (12 mg/dia com opção de reduzir para 9 mg/dia) e o grupo Paliperidona em estudo de dose flexível (doses entre 3 e 12 mg/dia, dose média modal de 8,6 mg/dia) cada um era superior ao placebo no PANSS.
No grupo de dose mais baixa do estudo de 2 níveis de dose (6 mg/dia com opção de reduzir para 3 mg/dia), Paliperidona não era significativamente diferente do placebo como avaliado pela PANSS.
Avaliando os resultados de ambos os estudos em conjunto, Paliperidona melhorou os sintomas do transtorno esquizoafetivo na avaliação final em relação ao placebo quando administrado em monoterapia ou em combinação com antidepressivos e/ou estabilizadores de humor.
Uma análise dos subgrupos da população não revelou nenhuma evidência de sensibilidade diferencial com base no sexo, idade ou região geográfica. Não havia dados suficientes para explorar os efeitos diferenciais baseados na raça.
Características farmacológicas
Propriedades Farmacodinâmicas
Mecanismo de ação
A paliperidona é um antagonista de ação central de receptores D2 da dopamina, com atividade antagonista serotonérgica 5-HT2A predominante. A paliperidona também é ativa como um antagonista em receptores adrenérgicos alfa-1 e alfa-2 e histaminérgicos H1.
A paliperidona não tem afinidade para receptores colinérgicos muscarínicos ou adrenérgicos beta-1 e beta-2. A atividade farmacológica dos enantiômeros (+) e (-) da paliperidona é similar, tanto qualitativamente como quantitativamente.
O mecanismo de ação da paliperidona, como outros fármacos eficazes em esquizofrenia, é desconhecido. No entanto, foi proposto que a atividade terapêutica do fármaco em esquizofrenia é mediada através da combinação de antagonismo em receptores tipo 2 (5HT2A) de serotonina e tipo 2 (D2) de dopamina.
O antagonismo em outros receptores além do D2 e 5HT2A pode explicar alguns dos outros efeitos da paliperidona.
O tempo médio estimado para o início da ação terapêutica do medicamento é de 4 a 8 dias.
Polisonografia
Medicamentos com ação central através de seu mecanismo de ação, perfil de liberação e/ou tempo da administração da dose podem afetar o sono. Para avaliar o impacto da dose matinal de Paliperidona sobre a arquitetura e a continuidade do sono, foi conduzido um estudo controlado com placebo em 36 pacientes com esquizofrenia onde 9 mg de Paliperidona ou placebo foram administrados uma vez ao dia por 14 dias.
As seguintes observações foram feitas (dados médios em comparação ao placebo) redução de 41,0 (EP 18,70) minutos na latência para sono persistente, diminuição de 35,2 (EP 14,99) minutos na latência para início do sono, redução de 7,0 (EP 3,88) eventos no número de vezes de despertar após o início do sono, aumento do tempo total de sono em 52,8 (SE 24,01) minutos, aumento do período de sono em 41,7 (SE 18,75) minutos e aumento do índice de eficiência do sono em 11,0% (SE 5,00).
Houve também uma redução estatisticamente significativa (em relação ao placebo) no estágio 1 do sono de 11,9 (SE 4,44) minutos e aumento no estágio 2 do sono de 50,7 (SE 17,67) minutos. Não foi observado efeito clinicamente relevante sobre o sono REM.
Efeito no intervalo QT/QTc e na eletrofisiologia cardíaca
Os efeitos da paliperidona sobre o intervalo QT foram avaliados em dois estudos de fase I, randomizados, duplocegos e multicêntricos, em adultos com esquizofrenia e transtorno esquizoafetivo e em 3 estudos de eficácia, de dose fixa, controlados com placebo e com controle ativo de 6 semanas de duração em adultos com esquizofrenia.
No primeiro estudo de fase I (n=141), pacientes foram randomizados para receber igualmente 7 dias de paliperidona oral de liberação imediata uma vez ao dia (com titulação de 4 a 8 mg) ou uma dose única de moxifloxacino (400mg).
A dose de 8 mg uma vez ao dia de paliperidona oral de liberação imediata (n=44) atingiu uma concentração plasmática média no estado de equilíbrio mais de 2 vezes maior que a exposição observada com dose máxima recomendada de 12 mg de Paliperidona (Cmáx ss= 113 e 45 ng/mL, respectivamente).
No modelo de correção “linear-derived QT correction” (QTcLD), houve um aumento médio de 5,5 mseg (90% IC: 3,66; 7,25) no grupo de tratamento com Paliperidona (n=44).
No segundo estudo de fase I (n=109), os pacientes foram randomizados para receber igualmente placebo, ou a dose máxima recomendada de Paliperidona (12 mg uma vez ao dia), subsequentemente titulado a uma dose acima da faixa recomendada (18 mg uma vez ao dia), ou um controle ativo da mesma classe farmacológica de medicamento (400 mg de quetiapina 2 vezes ao dia).
A comparação primária neste estudo de não inferioridade de 10 dias foi entre Paliperidona 12 mg e quetiapina. A média dos mínimos quadrados da condição basal QTcLD a cada um dos tmáx individuais observados foi estimada para ser 5,1 ms menor para Paliperidona 12 mg (Cmáx média 34 ng/mL) comparado com 400 mg de quetiapina 2 vezes ao dia (Cmáx média 1183 ng/mL) (IC 90%: -9,2; -0,9), encontrando o critério de não inferioridade pré-especificado de 10 ms.
A alteração média da condição basal em QTcLD para cada um dos tmáx individuais observados foi estimada para ser 2,3 ms menor para Paliperidona 18 mg (Cmáx média 53 ng/mL) comparado com 400 mg de quetiapina 2 vezes ao dia (Cmáx média 1183 ng/mL) (IC 90%: -6,8; 2,3).
A alteração média da condição basal em QTcLD para cada tmáx individual observado foi estimada para 1,5 ms maior (IC 90%: -3,3; 6,2) para Paliperidona 12 mg e 8,0 ms maior (IC 90%: 3,1; 12,9) para 400 mg de quetiapina 2 vezes ao dia comparado com alteração média da condição basal em QTcLD em um tmáx mediano observado (da droga ativa na comparação) no braço placebo concorrente.
A alteração média da condição basal em QTcLD para cada tmáx individual observado foi estimada para ser 4,9 ms maior (IC 90%: -0,05; 10,3) para paliperidona de liberação prolongada 18 mg e 7,5 ms maior (IC 90%: 2,5; 12,5) para quetiapina 400 mg duas vezes ao dia comparado com a alteração média da condição basal em QTcLD no tmáx mediano observado (da droga ativa na comparação) no braço placebo concorrente.
Nenhum dos pacientes tiveram mudanças da condição basal excedendo 60 mseg ou um QTcLD excedendo 500 mseg durante o tempo de duração de qualquer destes estudos.
Para os 3 estudos de eficácia de dose fixa, medidas eletrocardiográficas extensas foram coletadas em 15 tempos de avaliação em dias determinados (incluindo os tempos de Cmáx esperada), usando metodologia padronizada.
O aumento médio do QTcLD não excedeu 5 mseg em nenhum grupo de tratamento em nenhum tempo de avaliação, com base nos dados agrupados de 836 pacientes tratados com Paliperidona, 357 pacientes tratados com olanzapina e 350 pacientes tratados com placebo.
Um paciente no grupo Paliperidona 12 mg e um paciente no grupo olanzapina tiveram uma mudança que excedeu 60 mseg em um tempo de análise durante esses estudos (aumentos de 62 mseg e 110 mseg, respectivamente).
Propriedades Farmacocinéticas
As informações farmacocinéticas apresentadas a seguir são baseadas em dados de estudos em adultos, com exceção dos casos especificados.
A farmacocinética da paliperidona após a administração de Paliperidona, cuja forma farmacêutica corresponde à de comprimido revestido de liberação prolongada (OROS Push-Pull, tecnologia desenvolvida pela Alza Corporation) é proporcional à dose dentro do intervalo recomendado (3 a 12 mg).
Absorção
Após uma dose única de Paliperidona, as concentrações plasmáticas de paliperidona sobem constantemente até atingir o pico de concentração plasmática (Cmáx) em aproximadamente 24 horas após a administração. Com a administração de Paliperidona uma vez ao dia, as concentrações do estado de equilíbrio da paliperidona são atingidas em 4-5 dias na maioria dos indivíduos.
As características de liberação de Paliperidona resultam em flutuações mínimas do pico e de vale em comparação àquelas observadas com a risperidona de liberação imediata.
Em um estudo comparando a farmacocinética no estado de equilíbrio após a administração de 12 mg de paliperidona (comprimidos de liberação prolongada), uma vez ao dia, com 4 mg de risperidona de liberação imediata em pacientes com esquizofrenia, os índices de flutuação foram 38% para a paliperidona de liberação prolongada em comparação a 125% para a risperidona de liberação imediata.
Figura 1: Perfil de concentração no estado de equilíbrio após a administração de 12 mg de paliperidona (6 comprimidos de liberação prolongada de 2 mg, uma vez ao dia) por 6 dias (as concentrações de paliperidona estão representadas) em comparação a risperidona de liberação imediata administrada como 2 mg uma vez ao dia no Dia 1 e 4 mg uma vez ao dia nos Dias 2 a 6 (as concentrações de paliperidona+risperidona estão representadas):
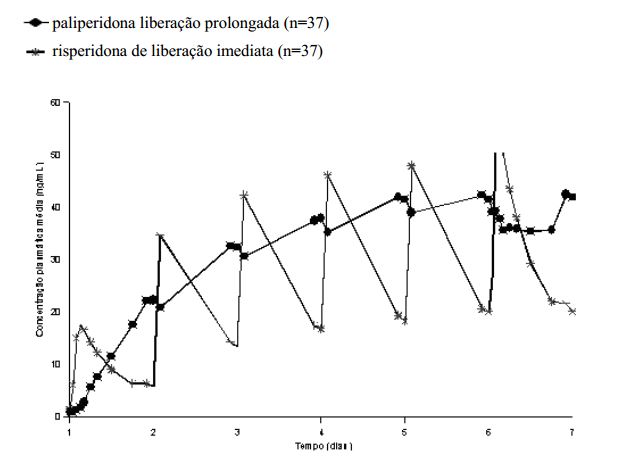
Após a administração de Paliperidona os enantiômeros (+) e (-) da paliperidona se interconvertem, alcançando uma razão de AUC (+) para (-) de aproximadamente 1,6 no estado de equilíbrio. A biodisponibilidade oral absoluta da paliperidona após a administração de Paliperidona é 28%.
Após a administração de um único comprimido de liberação prolongada de paliperidona a voluntários sadios, confinados ao leito por 36 horas, com refeição padrão com alto teor calórico/de gordura, a Cmáx e a AUC aumentaram em 42% e 46%, respectivamente, em comparação com a administração em condição de jejum.
Em outro estudo envolvendo voluntários sadios, após administração de um único comprimido de 12 mg em conjunto com uma refeição padronizada contendo elevado conteúdo de gordura e calorias, foram observados aumentos de 60% e 54% de Cmáx e AUC de paliperidona, respectivamente, comparados à administração em condições de jejum. Embora a presença ou ausência de alimentos no tempo de administração de Paliperidona possam aumentar ou diminuir a exposição à paliperidona, estas alterações não foram consideradas clinicamente relevantes.
Os estudos clínicos que estabeleceram a eficácia e a segurança de Paliperidona foram realizados sem relação com o tempo das refeições.
Distribuição
A paliperidona é rapidamente distribuída. O volume aparente de distribuição é 478 L. A ligação da paliperidona às proteínas plasmáticas é de 74%. Ela liga-se, principalmente, à glicoproteína alfa-1 ácida e à albumina.
Em condições in vitro, concentrações terapêuticas altas de diazepam (3 mcg/mL), sulfametazina (100 mcg/mL), varfarina (10 mcg/mL) e carbamazepina (10 mcg/mL) causaram um pequeno aumento na fração livre de paliperidona em 50 ng/mL. Não é esperado que essas mudanças tenham significância clínica.
Metabolismo e eliminação
Uma semana após a administração de uma dose oral única de 1 mg de 14C-paliperidona de liberação imediata, 59% da dose foi excretada inalterada na urina, indicando que a paliperidona não é extensivamente metabolizada no fígado. Aproximadamente 80% da radioatividade administrada foi recuperada na urina e 11% nas fezes.
Quatro vias metabólicas foram identificadas in vivo, nenhuma das quais representou mais de 6,5% da dose: desalquilação, hidroxilação, desidrogenação e cisão de benzisoxazol. Embora estudos in vivo tenham sugerido um papel para a CYP2D6 e a CYP3A4 no metabolismo da paliperidona, não há evidência in vivo de que essas isoenzimas representem um papel significativo no metabolismo da paliperidona.
Apesar da ampla variação na população em geral com relação à capacidade de metabolizar substratos de CYP2D6, as análises da farmacocinética da população não indicaram diferença perceptível na depuração aparente de paliperidona após a administração de Paliperidona entre metabolizadores rápidos e lentos de substratos de CYP2D6.
Estudos in vitro usando preparados de microssomas de sistemas heterólogos indicam que as CYP1A2, CYP2A6, CYP2C9, CYP2C19 e CYP3A5 não estão envolvidas no metabolismo da paliperidona. A meia-vida terminal de eliminação da paliperidona é cerca de 23 horas.
Insuficiência hepática
A paliperidona não é extensivamente metabolizada pelo fígado. Em um estudo em pacientes com insuficiência hepática moderada (Child-Pugh classe B), as concentrações plasmáticas da paliperidona livre foram similares àquelas em indivíduos sadios. A paliperidona não foi estudada em pacientes com insuficiência hepática grave.
Insuficiência renal
A dose deve ser reduzida em pacientes com insuficiência renal moderada e grave. A disposição da paliperidona foi estudada em pacientes com graus variáveis de insuficiência renal. A eliminação da paliperidona diminuiu com a diminuição da depuração da creatinina (DC).
A depuração total da paliperidona foi reduzida em pacientes com insuficiência renal
em 32% nos casos leves (DC = 50 a < 80 mL/min), 64% nos casos moderados (DC = 30 a < 50 mL/min) e 71% nos casos graves (DC = 10 a < 30 mL/min). A meia-vida de eliminação terminal da paliperidona foi 24, 40 e 51 horas em pacientes com insuficiência renal leve, moderada e grave, respectivamente, em comparação a 23 horas em indivíduos com a função renal normal (DC ≥ 80 mL/min).
Adolescentes
A exposição sistêmica à paliperidona em pacientes adolescentes foi comparável à exposição em adultos.
Em adolescentes com peso < 51 kg foi observada uma exposição 23% maior do que em adolescentes com peso ≥ 51 kg; este aumento não foi considerado clinicamente significativo. A idade, por si só, não influenciou na exposição à paliperidona.
Idosos
Os dados de um estudo de farmacocinética em indivíduos idosos (≥65 anos de idade, n=26) indicaram que a depuração aparente da paliperidona, no estado de equilíbrio após a administração de Paliperidona, foi 20% menor em comparação a indivíduos adultos (18-45 anos de idade, n=28).
No entanto, não houve efeito perceptível da idade na análise da farmacocinética da população envolvendo pacientes com esquizofrenia após a correção das reduções na depuração da creatinina relacionadas à idade.
Raça
Não é recomendado ajuste de dose com base na raça. A análise farmacocinética populacional não revelou evidências de diferenças relacionadas à raça na farmacocinética da paliperidona seguindo a administração de Paliperidona.
Em um estudo farmacocinético conduzido em japoneses e caucasianos não foram observadas diferenças na farmacocinética.
Sexo
A depuração aparente da paliperidona após a administração de Paliperidona é aproximadamente 19% menor em mulheres que em homens.
Essa diferença é amplamente explicada pelas diferenças na massa muscular corporal e na depuração da creatinina entre homens e mulheres, pois uma avaliação da farmacocinética da população não revelou evidência de diferenças clinicamente significativas relacionadas ao sexo na farmacocinética da paliperidona após a administração de Paliperidona, após correção para a massa muscular e a depuração de creatinina.
Tabagismo
Com base nos estudos in vitro utilizando enzimas hepáticas humanas, a paliperidona não é um substrato para a CYP1A2, portanto, o tabagismo, não deve afetar a farmacocinética da paliperidona.
Uma análise farmacocinética da população demonstrou haver uma exposição à paliperidona ligeiramente menor em fumantes do que em não-fumantes. No entanto, é improvável que esta diferença possua relevância clínica.
Dados de segurança pré-clinica
Toxicologia
Da mesma forma que outros fármacos antagonistas de receptores dopamina D2, a paliperidona elevou os níveis de prolactina sérica em estudos de toxicidade de dose repetida.
Em um estudo de toxicidade juvenil com 7 semanas de duração e doses orais de paliperdona de 0,16; 0,63 e 2,5 mg/dia, que correspondem, respectivamente, a 0,12; 0,5 e 1,8 vezes a dose máxima humana (12 mg/dia) recomendada para adolescentes em mg/m2, não foram observados efeitos no crescimento, maturidade sexual e desempenho reprodutivo.
Doses de até 2,5 mg/kg/dia não prejudicaram o desenvolvimento neurocomportamental em machos e fêmeas, exceto pelo efeito sobre a aprendizagem e memória em ratas fêmeas tratadas com 2,5 mg/kg/dia. Este efeito não foi observado após a descontinuação do tratamento.
Em um estudo com duração de 40 semanas em cães jovens tratados com ripseridona oral (que é extensivamente convertida a paliperidona) em doses de 0,31, 1,25, e 5 mg/kg/dia, a maturidade sexual não foi adversamente afetada com 0,31 e 1,25 mg/kg/dia. O crescimento de ossos longos não foi afetado com 0,31 mg/kg/dia; efeitos foram observados com 1,25 e 5 mg/kg/dia.
Carcinogenicidade
O potencial carcinogênico da paliperidona foi avaliado com base em estudos com a risperidona conduzidos em camundongos e ratos, uma vez que a paliperidona corresponde a um metabólito ativo da risperidona. A risperidona foi administrada em doses de até 10 mg/kg/dia por 18 meses em camundongos e 25 meses em ratos.
Houve aumentos estatisticamente significativos de adenomas de hipófise, adenomas de pâncreas endócrino e adenocarcinomas de glândulas mamárias. Um aumento de tumores mamários, hipofisários e de pâncreas endócrino foi encontrado em roedores após a administração crônica de outros antipsicóticos e é considerado como sendo mediado pelo antagonismo prolongado de dopamina D2. A relevância desses achados de tumores em roedores é desconhecida, em termos de risco para os seres humanos.
Mutagenicidade
Não foi encontrada evidência de potencial mutagênico para a paliperidona no teste de mutação reversa de Ames, no teste de linfoma de camundongo ou no teste de micronúcleo de rato.
Prejuízo da fertilidade
Embora o tratamento com a paliperidona tenha resultado em efeitos mediados pela prolactina e pelo sistema nervoso central, a fertilidade de ratos machos e fêmeas não foi afetada. Em uma dose materna tóxica, as fêmeas de ratos apresentaram um número ligeiramente menor de embriões vivos.
A embalagem de Invega Trinza® deve ser conservada em temperatura ambiente (entre 15ºC e 30ºC).
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Aspecto físico
Suspensão de liberação prolongada em seringas preenchidas. A suspensão é branca a quase branca.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
MS – 1.1236.3398
Farm. Resp.:
Erika Diago Rufino
CRF/SP n° 57.310
Registrado por:
Janssen-Cilag Farmacêutica Ltda.
Avenida Presidente Juscelino Kubitschek, 2041, São Paulo – SP
CNPJ 51.780.468/0001-87
Fabricado por:
Janssen Pharmaceutica N.V.
Beerse, Bélgica
Importado por:
Janssen-Cilag Farmacêutica Ltda.
Rodovia Presidente Dutra, km 154
São José dos Campos – SP
CNPJ 51.780.468/0002-68
® Marca Registrada
Venda sob prescrição médica.
Só pode ser vendido com retenção da receita.
Especificações sobre o Invega Trinza
Caracteristicas Principais
Fabricante:
Tipo do Medicamento:
Novo
Necessita de Receita:
C1 Branca 2 vias (Venda Sob Prescrição Médica - Este medicamento pode causar Dependência Física ou Psíquica)
Principio Ativo:
Categoria do Medicamento:
Classe Terapêutica:
Especialidades:
Psicanálise
Psiquiatria
Psicologia
Preço Máximo ao Consumidor:
PMC/SP R$ 11.373,80
Preço de Fábrica:
PF/SP R$ 8.536,91
Registro no Ministério da Saúde:
1123633980197
Código de Barras:
7896212425730
Temperatura de Armazenamento:
Temperatura ambiente
Produto Refrigerado:
Este produto não precisa ser refrigerado
Doenças Relacionadas:
Bula do Paciente:
Bula do Profissional:
Modo de Uso:
Uso injetável
Pode partir:
Esta apresentação não pode ser partida
INVEGA TRINZA É UM MEDICAMENTO. SEU USO PODE TRAZER RISCOS. PROCURE UM MÉDICO OU UM FARMACÊUTICO. LEIA A BULA. MEDICAMENTOS PODEM CAUSAR EFEITOS INDESEJADOS. EVITE A AUTOMEDICAÇÃO: INFORME-SE COM SEU MÉDICO OU FARMACÊUTICO.
Descubra a Melhor Opção de Invega Trinza para Você
Compare e escolha entre variações com facilidade
 | ||||
| Invega Trinza 200mg/mL, caixa com seringa preenchida com 0,875mL de suspensão injetável de liberação prolongada + 2 agulhas | Invega Trinza 200mg/mL, caixa com seringa preenchida com 1,315mL de suspensão injetável de liberação prolongada + 2 agulhas | Invega Trinza 200mg/mL, caixa com seringa preenchida com 1,750mL de suspensão injetável de liberação prolongada + 2 agulhas | Invega Trinza 200mg/mL, caixa com seringa preenchida com 2,625mL de suspensão injetável de liberação prolongada + 2 agulhas | |
Dose | 200mg/mL | 263mg | 350mg | 200mg/mL |
Forma Farmacêutica | Suspensão injetável | Suspensão injetável | Suspensão injetável | Suspensão injetável |
Quantidade na embalagem | 0.875 mL | 1.315 mL | 1.75 mL | 2.625 mL |
Modo de uso | Uso injetável | Uso injetável | Uso injetável | Uso injetável |
Substância ativa | Paliperidona | Paliperidona | Paliperidona | Paliperidona |
Preço Máximo ao Consumidor/SP | R$ 5.238,18 | R$ 7.872,22 | R$ 10.476,35 | R$ 11.373,80 |
Preço de Fábrica/SP | R$ 3.931,66 | R$ 5.908,71 | R$ 7.863,31 | R$ 8.536,91 |
Tipo do Medicamento | Novo | Novo | Novo | Novo |
Pode partir? | Este medicamento não pode ser partido | Este medicamento não pode ser partido | Este medicamento não pode ser partido | Este medicamento não pode ser partido |
Registro Anvisa | 1123633980162 | 1123633980170 | 1123633980189 | 1123633980197 |
Precisa de receita | Sim, precisa de receita | Sim, precisa de receita | Sim, precisa de receita | Sim, precisa de receita |
Tipo da Receita | C1 Branca 2 vias (Venda Sob Prescrição Médica - Este medicamento pode causar Dependência Física ou Psíquica) | C1 Branca 2 vias (Venda Sob Prescrição Médica - Este medicamento pode causar Dependência Física ou Psíquica) | C1 Branca 2 vias (Venda Sob Prescrição Médica - Este medicamento pode causar Dependência Física ou Psíquica) | C1 Branca 2 vias (Venda Sob Prescrição Médica - Este medicamento pode causar Dependência Física ou Psíquica) |
Código de Barras | 7896212425648 | 7896212425679 | 7896212425709 | 7896212425730 |
















